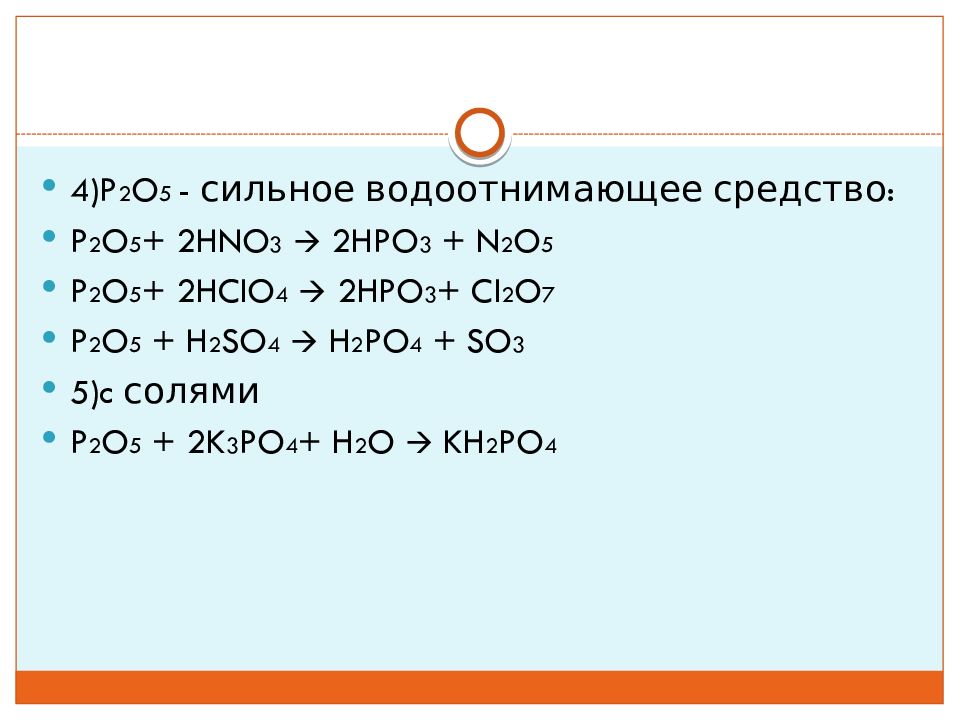
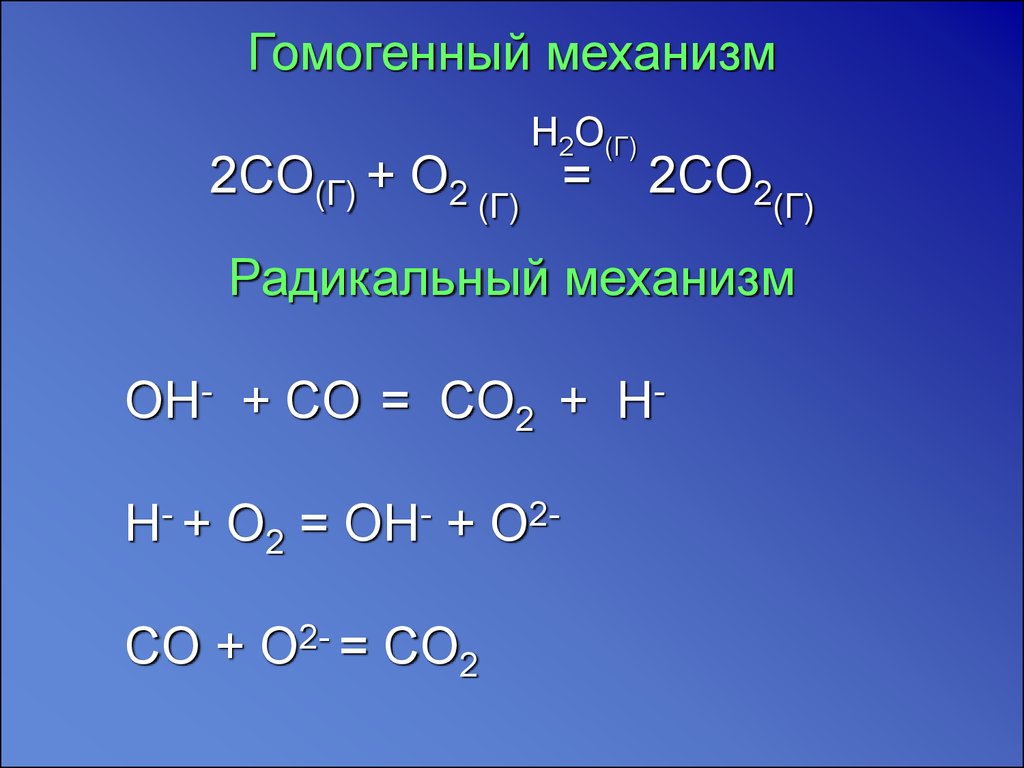
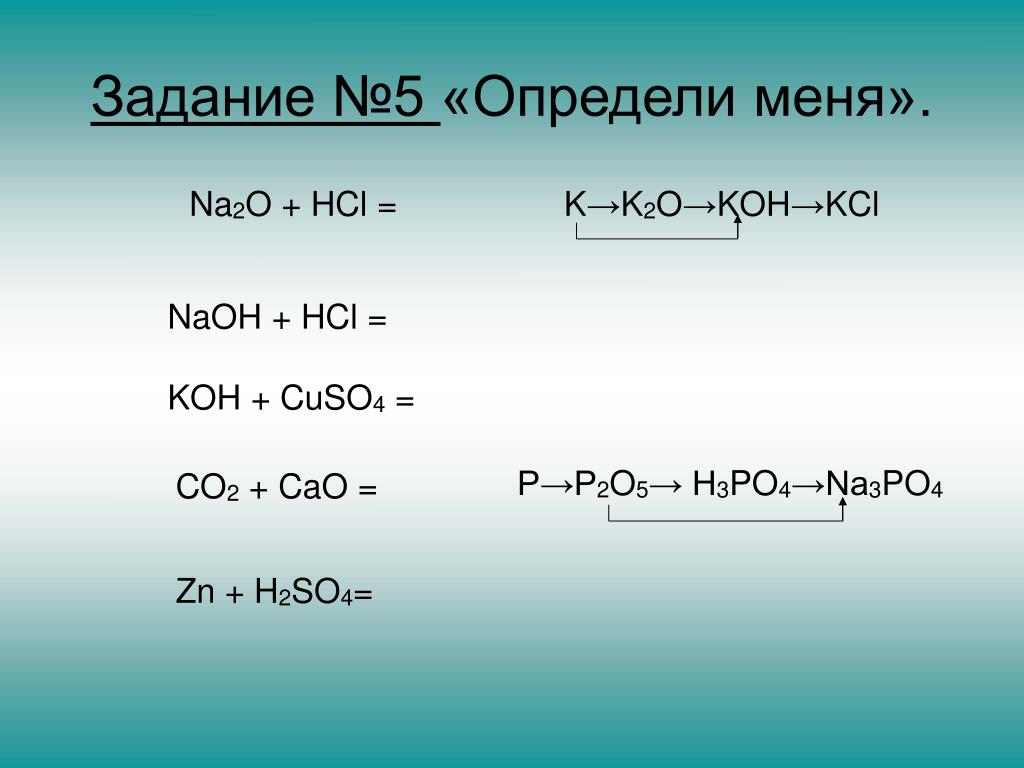
Co+o2. P o2 co2. P o2 co2. C o2 co2 окислительно восстановительная. выберите формулы оксидов. формулы оксидов 8 класс. P o2 co2. с02 это кислотный оксид. Co2+ o2. экзотермическая реакция это в химии 8 класс. Co2+h2. Co+o2. P2o5 реакции. окислительно-восстановительные реакции неметаллов. Koh co2 реакция. P o2 co2. экзотермическая реакция протекает с. P2o5+h2o химическое реакция. Koh+h2so4 уравнение. H2co3 это газ. распределить оксиды по группам. P o2 p2o5 окислительно восстановительная реакция. P o2 co2. Na2co3 реакция. Co+o2. экзотермическая реакция. Co o2 co2. P o2 co2. So2 p2o5. взаимодействие кислорода со сложными веществами. распределите по группам следующие оксиды na2o, co2. формула оксидов в химии. Fe oh 3 hcl. Co o2 co2. P o2 co2. Co2 кислота. P o2 co2. 4p 5o2 2p2o5 электронный баланс. Si+cl2. Co2 c 2co овр. Co2 окислительно восстановительная реакция. угольная кислота h2co3. Fe(oh)3. Co2. H2co3 распадается. формула p2o5 + h2o. C12h22o11 h2o. H2co3 угольная кислота co2. свойства оксидов в ряду. Cl2 + 2p. Ph3 co2. P o2 co2. P o2 co2. Nano2 hcl. Fe2o3 co2 h2o. кислотно-основные свойства оксидов. P p2o5 овр. взаимодействие веществ с кислородом co +o2. P2o5 c p co окислительно восстановительная реакция. способы получения основных оксидов. P4+o2. Co2+02. P2o5+c электронный баланс. 2co+o2 2co2. Cr2o3 оксид. C co2 h2co3 na2co3 цепочка. P o2 co2. H2co3. Co2+h2o. P o2 co2. Si ca ca2si электронный баланс. способы полученияосновыных окстдов. взаимодействие простых и сложных веществ с кислородом. P o2 co2. P o2 co2. P co2. Co+o2 овр. уравнения взаимодействия кислорода со сложными веществами. P2o5 c p co окислительно восстановительная. 2h2so4. P o2 co2. способы получения кислотных оксидов. C o2 co2 овр. формулы основных оксидов. экзщотермичные реакции. распределите по группам следующие оксиды co. Koh + h2so4 -> фф. P o2 co2. P o2 co2. Co2+o2. P o2 co2. Co h2 реакция. Co2+02. основные и кислотные свойства высших оксидов. P o2 co2. Co2+o2. Caco3 cao co2 реакция разложения. выберите уравнения реакций разложения. P o2 co2. от кислотных к основным меняются свойства оксидов в ряду.